Introduction
Le sepsis est un syndrome infectieux grave qui se caractérise par une dysfonction d’organe liée à une infection.
Il est la principale cause de décès dans les infections et sa prise en charge doit être rapide.
Le choc septique est un sepsis qui ne répond pas à la prise en charge initiale et nécessite l’administration de vasopresseurs.
Définitions
= présence de signes inflammatoires cliniques et/ou biologiques liés à un agent infectieux.
infection associée à une défaillance d’organe.
= sepsis avec hypotension persistante malgré un remplissage vasculaire adapté + hyperlactatémie > 2 mmol/l.
I. Étapes clinique
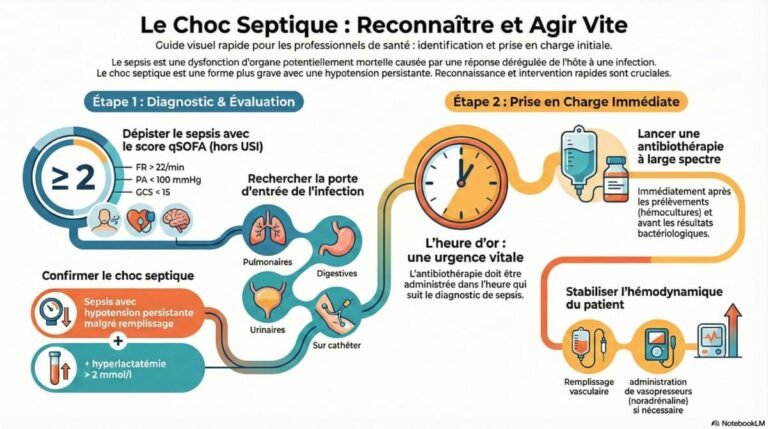
Rechercher un sepsis devant toute infection (qSOFA / SOFA)
Utiliser le score qSOFA pour dépister rapidement le sepsis (hors USI)
- FR > 22
- PA < 100
- GCS < 15
qSOFA ≥ 2 suggère un sepsis et nécessite une prise en charge spécifique.
Les marbrures, bien que non incluses dans le qSOFA, sont un signe de gravité à rechercher.
En USI on utilise le score SOFA (risque de mortalité si SOFA = 2 ou +) :
Sequential Organe Failure Assesment (6 items) Notés de 0 à 4
Respiratoire / cardio Vasculaire / rénal
Hépatique / SNC / coagulation
- Respiratoire 🫁 PaO2/FiO2 < 400 ⇒ 1 pt et 2 pts si < 300 (…)
- Cardio-vasculaire🫀 : 1 pt si PAM < 70 et 2 pts si amines …
- Hépatique : bilirubine (1 pt si Bilirubine > 12 mmol/L et 2 pts si > 19)
- Sanguin : plaquettes (1 pt si < 150 G/L et 2 pts si < 101 G/L)
- Neurologique : GCS < 15 (1 pt pour GCS = 13 – 14 et 2 pts si < 12)
- Rénal : ↗️ créatinine (1 pt si > 110 et 2 pts si > 170) ou ↘️ diurèse (oligurie = 3 pts; anurie = 4 pts)
Un score SOFA ≥ 2 ⇒ risque de mortalité
Rechercher une porte d'entrée
Déterminer la source de l’infection pour orienter le traitement.
Les portes d’entrée les plus fréquentes sont les infections pulmonaires, digestives, urinaires, sur cathéter et des parties molles.
Cas du purpura fulminans
Devant un sepsis suspecté, rechercher un purpura nécrotique ou ecchymotique de plus de 3 mm.
En cas de purpura fulminans, injecter immédiatement 2 g de ceftriaxone ou de céfotaxime (= C3G) et transférer le patient en réanimation.
II. Examens complémentaires
Évaluer le retentissement de l’infection : gaz du sang, lactate, bilan hépatique, NFS, bilan d’hémostase, ionogramme.
Préciser l’étiologie : hémocultures, prélèvements et imagerie ciblés.
Place des biomarqueurs (procalcitonine et CRP) : peu utiles pour le diagnostic de sepsis.
L’usage de la PCT est utile pour l’arrêt de l’antibiothérapie.
III. Mesures thérapeutiques immédiates
1 – Avis du réanimateur.
2 – Prise en charge des défaillances d’organe : stabilisation hémodynamique, respiratoire et rénale.
3 – Contrôle de l’infection ⇒ Antibiothérapie d’urgence (= immédiate dans le purpura fulminans et dans l’heure pour le reste, juste après prélèvement des hémocultures) à plus large spectre possible puis éventuelle désescalade après 48 h (si amélioration clinique et résultats bactériologiques compatibles).
Repères pour une antibiothérapie d'urgence
Germes :
Streptococcus pneumoniae et Legionella pneumophila
Les Staphylococcus aureus, entérobactéries, Haemophilus influenzae, Mycoplasma pneumoniae, Chlamydia pneumoniae sont moins fréquents. Prendre en compte les anaérobies en cas d’inhalation
Céfotaxime ou ceftriaxone + atb actif sur les germes intra cellulaires (macrolides IV) ou FQ anti pneumocoque (lévofloxacine 500 mg x2 IVL)
Si facteur de risque de pseudomonas (BPCO stade IV ayant eu des atb au cours des 6 mois précédents, bronchectasie ou mucoviscidose).
⇒TAZO 4g x3 ou 4/j ou céfépime 1 – 2g x3/j = C4G antipseudomonas
ou carbapénème (imipenème, méropénème, ertapénème) = spectre très large y compris les BGN producteurs de bêta lactamases étendue + amikacine + atb actif sur les germes intra cellulaires (macrolides ou tétracyclines).
Germes :
Entérobactéries, S. Aureus (qui peut être Méticilline Résistant = SARM), P. Aeruginosa, A. Baumanii
Polymicrobiennes dans 30% des cas.
Traitement empirique initial
Cas précoces (<5 jours) sans facteurs de risque :
- Amoxicilline-Acide Clavulanique (1 g x3 /j)
- Pipéracilline-tazobactam 4.5 g x4/j
Cas tardifs ou facteurs de résistance :
- Carbapénème (imipenème 500mg x4/j ou méropénème 1g x3/j) + amikacine 15-20 mg/kg/j
- En cas de résistance aux carbapénèmes >20% : Ceftazidime-avibactam 2.5 g x3/j + aztreonam 2g x3/j
Adaptation thérapeutique (selon le germe)
Pseudomonas aeruginosa :
- Association β-lactamine (pipéracilline-tazobactam, céfépime) + amikacine
- En cas de résistance : colistine 9 MUI x2/j en nébulisation
Acinetobacter baumannii :
SARM (Staphylococcus Aureus Méticilline Résistant):
- Linézolide 600mg x2/j (privilégié en cas d’atteinte pulmonaire isolée)
- Vancomycine (30 mg/kg/24h en perfusion ou cibles d’ASC >400 mg.h/L)
Germes :
Escherichia coli, Proteus, Klebsiella, entérocoques
⇒ céfotaxime ou ceftriaxone (aztréonam si allergie) + amikacine
Si infection urinaire nosocomiale / associée aux soins ⇒ carbapénème + amikacine
Germes :
Escherichia coli, entérobactéries, Bacteroides fragilis, entérocoques
Pipéracilline-tazobactam et gentamicine
+ traitement antifongique type échinocandines (anidulafungine, caspofungine, micafungine ou rezafungine) si défaillance hémodynamique, sexe féminin, ou chirurgie sus-mésocolique, atb > 48h
Germes :
Streptocoques, staphylocoques, anaérobies, entérobactéries dans les localisations périnéales
- Membres, tête et cou : amoxicilline-acide clavulanique
- Périnée : pipéracilline-tazobactam + Linézolide si portage ou risque de Staphylococcus aureus résistant à la méticilline.
Céfotaxime / ceftriaxone + gentamicine
Si infection nosocomiale :
Carbapénème ou Pipéracilline/tazobactam + amikacine ± vancomycine ou linézolide si suspicion de staphylocoque (dispositif vasculaire)
IV. Mesures thérapeutiques spécialisées
Surveillance continue et réévaluation.
Support vasopresseur (noradrénaline) d’emblée si PA diastolique < 40 mmHg ou si échec du remplissage à maintenir une PAM à 65 mmHg
Prise en charge des défaillances d’organes.
Contrôle du foyer infectieux (drainage chirurgical ou endoscopique du foyer infectieux, excision des tissus nécrotiques, ablation d’un dispositif d’abord vasculaire infecté).
V. Points de vigilance
Considérer un sepsis comme une urgence vitale.
Administrer l’antibiothérapie dans l’heure chez tout patient en sepsis.
Rechercher et traiter un foyer infectieux.
Réévaluer l’efficacité du traitement.
Avis du réanimateur dès le stade de suspicion de sepsis.
Publication : janvier 2026

Vous devez être connecté pour poster un commentaire.